Matura z chemii 2012 - poziom rozszerzony
rozwiązania ze szczegółowym opracowaniem
Zadanie 1.
Atomy pierwiastka X tworzą kationy X2+ o następującej konfiguracji elektronowej:
1s2 2s2 2p6 3s2 3p6 3d10
Podaj symbol pierwiastka X, określ jego położenie w układzie okresowym i blok energetyczny (konfiguracyjny), do którego pierwiastek ten należy. 
[Skoro dwudodatni kation pierwiastka X ma 28 elektronów (sumujemy liczby w górnych indeksach w konfiguracji elektronowej), to atom ma 30 elektronów (o 2 elektrony więcej). Liczba elektronów w atomie (ale nie w jonie) jest równa liczbie protonów i jest równa liczbie atomowej. Pierwiastek o liczbie atomowej 30 to cynk.
Cynk ma symbol Zn, leży w czwartym okresie, w 12 grupie, w bloku d. Alternatywnie informacje można wnioskować z konfiguracji elektronowej atomu (1s2 2s2 2p6 3s2 3p6 4s2 3d10). Najwyższy występujący tu numer powłoki wynosi 4, zatem atom ma 4 powłoki, więc leży w czwartym okresie. Liczba elektronów walencyjnych wynosi 12 (2+10), więc numer grupy to 12. Elektrony walencyjne znajdują się na podpowłoce s czwartej powłoki i na podpowłoce d trzeciej powłoki - z tego wynika, że jest to pierwiastek bloku d.]
Zadanie 2.
Pewien orbital atomowy opisują liczby kwantowe o następujących wartościach: główna liczba kwantowa n = 4 poboczna liczba kwantowa l = 2 magnetyczna liczba kwantowa ml = 0
Uzupełnij poniższe zdanie, wybierając symbol podpowłoki, do której należy ten orbital, oraz maksymalną liczbę elektronów na tej podpowłoce. Podkreśl wybrany symbol podpowłoki i liczbę elektronów.
Opisany orbital należy do podpowłoki ( 4s / 4p / 4d / 4f ), na której maksymalna liczba elektronów wynosi ( 2 / 6 / 10 / 14 ).
Zadanie 3.
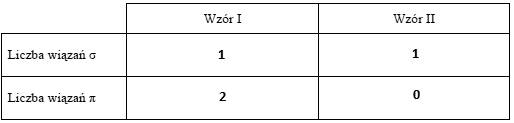
Poniżej przedstawiono wzory elektronowe dwóch cząsteczek.

Określ liczbę wiązań sigma i pi w cząsteczkach, których budowę elektronową ilustrują oba wzory.
Zadanie 4.
Poniższy schemat przedstawia początkowy fragment szeregu promieniotwórczego toru. Numerami w kółkach oznaczono kolejne nuklidy, a strzałkami przemiany jądrowe, jakim te nuklidy ulegają.
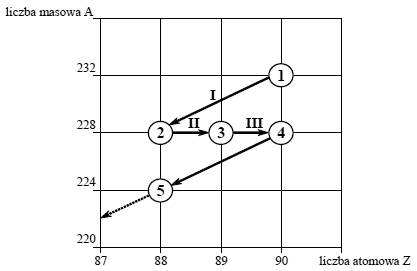
Napisz równanie przemiany jądrowej oznaczonej na schemacie numerem III. Podaj symbole oraz wartości liczby masowej i liczby atomowej jąder, będących substratami i produktami tej przemiany.
![]()
Zadanie 5.
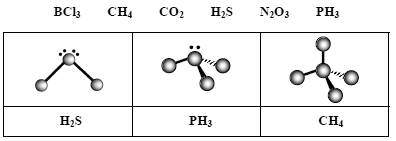
Poniżej zamieszczono schematy ilustrujące budowę cząsteczek wybranych związków kowalencyjnych (schematy nie uwzględniają proporcji rozmiarów atomów). Każdemu schematowi przyporządkuj wzór związku chemicznego, którego cząsteczkom można przypisać geometrię zilustrowaną tym schematem. Wzory wybierz spośród następujących:
Zadanie 6.
W dwóch probówkach oznaczonych numerami I i II umieszczono taką samą ilość wiórków magnezowych. Następnie do probówek wprowadzono jednakowe objętości kwasu solnego o temperaturze 25 stopni C ale różnych stężeniach. Przebieg doświadczenia ilustruje poniższy rysunek.
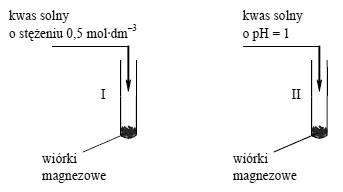
Napisz numer probówki, w której reakcja kwasu solnego z magnezem zaszła szybciej.
Rozwiązanie
Reakcja zaszła szybciej w tej probówce, do której wlano kwas o wyższym stężeniu. Aby porównać stężenia kwasu w obu probówkach, obliczamy stężenie molowe w probówce II na podstawie pH. Skoro pH=1 to stężenie jonów H+ wynosi 10-1 mol/dm3, czyli 0,1 mol/dm3. Z definicji:
pH = -log[H+] <==> [H+] = 10-pH
Kwas solny dysocjuje całkowicie i jest kwasem jednoprotonowym HCl → H+ + Cl- zatem stężenie molowe kwasu jest równe stężeniu jonów H+.
Stężenie molowe kwasu w probówce II wynosi w takim razie 0,1 mol/dm3 i jest niższe od stężenia kwasu w probówce I.
Reakcja zaszła szybciej w probówce numer I.
Zadanie 7.
Poniżej podano wartości standardowej entalpii tworzenia trzech związków chemicznych.

Korzystając z powyższych danych, oblicz wartość entalpii reakcji rozkładu 50 gramów węglanu wapnia, która zachodzi zgodnie z równaniem
CaCO3 (s) → CaO (s) + CO2 (g)
Obliczenia:
reakcja 1:
C (s) + O2 (g) --> CO2 (g)
![]() H01 = -394 kJ
H01 = -394 kJ
reakcja 2:
Ca (s) + 1/2 O2 (g) --> CaO (s)
![]() H02 = -635 kJ
H02 = -635 kJ
reakcja 3:
Ca (s)+ C (s) + 3/2 O2 (g) --> CaCO3 (s)
![]() H03 = -1207 kJ
H03 = -1207 kJ
reakcja 4:
CaCO3 (s) --> Ca (s) + C + 3/2 O2 (g)
![]() H04 = 1207 kJ
H04 = 1207 kJ
MCaCO3 = (40 + 12 + 3*16) g/mol = 100 g/mol nCaCO3 = (50 g)/ (100 g/mol) = 1/2 mol
Entalpia reakcji: 1/2 CaCO3 (s) →1/2 CaO (s) + 1/2 CO2 (g) stanowi połowę sumy entalpii reakcji 4, entalpii reakcji 1 i entalpii reakcji 2.
![]() H05 = 1/2 (1207 kJ - 394 kJ - 635 kJ)
H05 = 1/2 (1207 kJ - 394 kJ - 635 kJ)
![]() H05 = 89 kJ
H05 = 89 kJ
Odpowiedź: Entalpia reakcji rozkładu 50 gramów węglanu wapnia wynosi 89 kJ.
[W tym zadaniu tak "manewrujemy" reakcjami, aby "złożyć" reakcję, której entalpię mamy obliczyć z innych reakcji, których entalpie znamy albo możemy łatwo obliczyć. Wykonujemy zabiegi formalne, takie jak zapisanie reakcji przeciwnej do danej, pomnożenie obu stron równania przez liczbę czy też zsumowanie kilku reakcji. Wykonując te przekształcenia "nie martwimy się" o to, czy dana przemiana jest praktycznie przeprowadzalna - to zabiegi abstrakcyjne. Dla przypomnienia: entalpia jest funkcją stanu i nie zależy od drogi, ważny jest stan początkowy i stan końcowy. W oparciu o to założenie "manewrujemy" reakcjami.]
Zadanie 8.
W dwóch probówkach znajdowała się woda destylowana o temperaturze 25 stopni C. Do probówki I wprowadzono pewną liczbę moli soli A, a do probówki II - taką samą liczbę moli soli B. Stwierdzono, że w probówce I powstały roztwór jest cieplejszy od użytej wody destylowanej, natomiast zawartość probówki II nieco ochłodziła się w czasie rozpuszczania w niej soli B.
Wiedząc, że do przygotowania roztworów użyto chlorku magnezu i azotanu(V) amonu, a standardowe entalpie rozpuszczania w wodzie tych soli wynoszą
![]() napisz wzór soli, której roztwór otrzymano w probówce I.
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii,
Warszawa 2007
napisz wzór soli, której roztwór otrzymano w probówce I.
Na podstawie: K.-H. Lautenschläger, W. Schröter, A. Wanninger, Nowoczesne kompendium chemii,
Warszawa 2007
W probówce I otrzymano roztwór MgCl2
[Ujemna wartość entalpii oznacza proces egzoenergetyczny, czyli taki, który przebiega z wydzieleniem energii do otoczenia, dodatnia wartość entalpii oznacza proces endoenergetyczny, czyli przebiegający z pobraniem energii z otoczenia. Ogrzanie się zawartości probówki oznacza, że wydzieliła się energia na sposób ciepła, ochłodzenie - że została pobrana energia na sposób ciepła.]
Zadanie 9.
W pewnych warunkach temperatury i ciśnienia, innych niż warunki normalne, odmierzono 1,00 dm3 gazowego paliwa, którego 55% objętości stanowił propan, 44% objętości stanowił butan, a 1% objętości - składniki niepalne.
Oblicz objętość tlenku węgla(IV), który powstanie w tych samych warunkach temperatury i ciśnienia w wyniku całkowitego spalenia odmierzonej objętości paliwa zgodnie z równaniami C3H8 + 5O2 → 3CO2 + 4H2O i 2C4H10 + 13O2 → 8CO2 + 10H2O
Wynik podaj z dokładnością do drugiego miejsca po przecinku.
Obliczenia:
Vpaliwa = 1 dm3 V C3H8 = 0,55 * 1 dm3 = 0,55 dm3 V C4H10 = 0,44 * 1 dm3 = 0,44 dm3
VCO2 = ?
Z prawa Avogadra wynika, że stosunek liczby moli gazu ulegającego spalaniu do liczby moli powstającego dwutlenku węgla jest równy stosunkowi objętości gazu ulegającego spalaniu do objętości powstającego dwutlenku węgla. Zatem na podstawie współczynników stechiometrycznych przy odpowiednich reagentach w równaniach reakcji:
1 dm3 C3H8 ----- 3 dm3 CO2 0,55 dm3 C3H8 ------ x [dm3] CO2
x = (0,55 dm3 * 3 dm3)/(1 dm3) x = 1,65 dm3
2 dm3 C4H10 ----- 8 dm3 CO2 0,44 dm3 C4H10 ------ y [dm3] CO2
y = (0,44 dm3 * 8 dm3)/(2 dm3) y = 1,76 dm3
Vcałk CO2 = x + y Vcałk CO2 = 1,65 dm3 + 1,76 dm3 Vcałk CO2 = 3,41 dm3 Odpowiedź: Powstanie 3,41 dm3 dwutlenku węgla.
Informacja do zadań 10. i 11. W poniższej tabeli podano wzory wszystkich kationów i anionów, których obecność stwierdzono w badanym roztworze wodnym, oraz wartości stężenia tych jonów - z wyjątkiem anionów siarczanowych(VI).
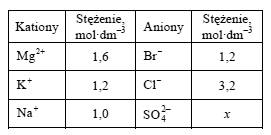
Zadanie 10.
Wiedząc, że każdy roztwór jest elektrycznie obojętny, ustal wartość stężenia molowego x anionów siarczanowych(VI) w badanym roztworze. Wynik podaj z dokładnością do jednego miejsca po przecinku.
2*1,6 + 1,2 + 1,0 - (1,2 + 3,2 + 2*x) = 0 5,4 - 4,4 - 2*x = 0 2*x = 1,0 x = 0,5 [SO42-] = 0,5 mol/dm3
Zadanie 11.
Próbkę badanego roztworu (o składzie podanym w tabeli) poddano działaniu chloru. W wyniku reakcji roztwór zabarwił się na kolor żółtopomarańczowy. Substancją, która spowodowała to zabarwienie, była czerwonobrunatna lotna ciecz o charakterystycznym ostrym zapachu. Substancja ta reaguje z większością metali oraz niektórymi niemetalami, a także z nienasyconymi związkami organicznymi.
Napisz w formie jonowej skróconej równanie reakcji odpowiedniego składnika badanego roztworu z chlorem, w wyniku której powstała opisana substancja.
2 Br- + Cl2 → Br2 + 2 Cl-
Zadanie 12.
a) Uzupełnij tabelę, wpisując wartość stężenia jonów OH- oraz wartość pH i pOH roztworu wodnego, w którym stężenie jonów H+ jest równe 10-9 mol*dm-3.

[H+]*[OH-] = 10-14 [OH-] = 10-14 / 10-9 [OH-] = 10-5 pH = -log[H+]10-9 pH = 9 pOH = -log[OH-] pOH = -log10-5 pOH = 5
Obliczone wartości wpisujemy do tabeli.
b) Określ odczyn opisanego roztworu.
Odczyn roztworu jest zasadowy.
Zadanie 13.
Do 150,00 cm3 wodnego roztworu NaOH o stężeniu 0,54 mol*dm-3 dodano 50,00 cm3 kwasu solnego o stężeniu 2,02 mol*dm-3. Oblicz pH otrzymanego roztworu.
Obliczenia:
V NaOH = 150,00 cm3 C NaOH = 0,54 mol*dm-3 V HCl = 50,00 cm3 C HCl = 2,02 mol*dm-3 pH = ?
Cm = n/V n = C*V n NaOH = 0,54 mol*dm-3 * 0,150 dm3 n NaOH = 0,081 mol n HCl = 2,02 mol*dm-3*0,050 cm3 n HCl = 0,101 mol
NaOH + HCl → NaCl + H2O
Z równiania reakcji widać, że 1 mol wodorotlenku sodu reaguje z jednym molem kwasu solnego. Zatem HCl użyto w nadmiarze. Obliczam liczbę moli kwasu, który przereagował:
1 mol NaOH ----- 1 mol HCl 0,081 mol NaOH ----- x [mol] HCl
x = 0,081 mol
Obliczam liczbę moli kwasu, który nie przereagował: y = 0,101 mol - 0,081 mol C końc HCl = (0,020 mol)/(0,150 dm3 + 0,050 dm3) [Dzielę "liczbę moli" kwasu przez objętość końcowego roztworu (zakładam addytywność objętości) i sumuję objętości użytych roztworów] C końc HCl = (0,020 mol)/(0,200 dm3) C końc HCl = 0,1 mol/dm3
HCl jest kwasem jednoprotonowym dysocjującym praktycznie całkowicie, zatem stężenie molowe kationów wodoru w końcowym roztworze jest równe końcowemu stężeniu molowemu kwasu solnego: [H+] = C końc HCl [H+] = 0,1 mol/dm3
pH = -log[H+] pH = -log0,1 pH=1
Odpowiedź: pH otrzymanego roztworu wynosi 1.
Zadanie 14.
Związek między mocą kwasu Brönsteda i sprzężonej z tym kwasem zasady w roztworach wodnych przedstawia zależność: Ka * Kb = Kw gdzie Ka oznacza stałą dysocjacji kwasu, Kb stałą dysocjacji sprzężonej zasady, a Kw iloczyn jonowy wody, którego wartość wynosi 1,0 * 10-14 w temperaturze 298 K. W poniższej tabeli podano wartości stałej dysocjacji wybranych kwasów w temperaturze 298 K.
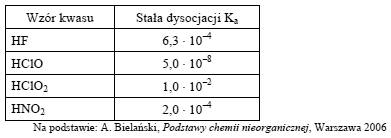
Na podstawie powyższej informacji napisz wzory zasad sprzężonych z kwasami wymienionymi w tabeli uporządkowane od najsłabszej do najmocniejszej.

Szereguję pomocniczo najpierw kwasy według rosnącej mocy. Im wyższa wartość stałej dysocjacji, tym mocniejszy kwas.
HClO, HNO2, HF, HClO2
Moc zasad sprzężonych z powyższymi kwasami wzrasta w odwrotnej kolejności: ClO2-, F-, NO2-, ClO-
Informacja do zadań 15.-16. W reakcji wodnego roztworu chlorku kobaltu(II) z wodnym roztworem wodorotlenku sodu najpierw powstaje niebieski osad hydroksosoli: chlorku wodorotlenku kobaltu(II) o wzorze Co(OH)Cl. Związek ten pod wpływem kolejnych porcji roztworu wodorotlenku sodu przechodzi w różowy osad wodorotlenku kobaltu(II), który praktycznie nie rozpuszcza się w nadmiarze tego odczynnika, ale brunatnieje wskutek utleniania obecnym w powietrzu tlenem. Opisane przemiany ilustruje poniższy schemat.
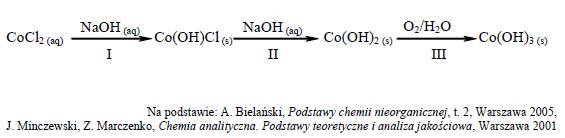
Zadanie 15.
a) Napisz w formie jonowej skróconej równania reakcji oznaczonych numerami I i II.
I Co2+ + Cl- + OH- → Co(OH)Cl
II Co(OH)Cl + OH- → Co(OH)2 + Cl-
b) Napisz w formie cząsteczkowej równanie reakcji oznaczonej numerem III.
III 4 Co(OH)2 + O2 + 2 H2O → 4 Co(OH)3
Zadanie 16.
Określ charakter chemiczny (kwasowo-zasadowy) wodorotlenku kobaltu(II).
Zasadowy. [Niektóre źródła podają, że wodorotlenek kobaltu(II) jest amfoteryczny.]
